基于PLGA的纳米医生制造:技术概述和工业扩展中的挑战
以聚乳酸-羟基乙酸(PLGA)为载体的纳米药物为生物医学研究提供了巨大的机遇。尽管几种基于PLGA的系统已经获得了美国食品药品管理局(FDA)和欧洲药品管理局(EMA)的批准,并被广泛用于疾病的临床治疗或诊断,但目前全球市场上没有PLGA纳米药物配方。
最大的障碍之一是开发一种制造技术,使纳米药物生产能够从实验室转移到具有适当特性和质量控制方法的工业规模。
本综述提供了基于PLGA纳米粒子的聚合物纳米胺的制造和分析的技术概述,妨碍其工业实用性的扩大挑战以及与其成功翻译成临床实践相关的问题。
介绍
纳米技术是最有前途的关键促进技术(KETS),可以为社会的未满足需求提供创新和激进的解决方案(Soares等,2018,Tinkle等,2014)。如今,纳米技术触动了人类生命的各个方面,包括医学,引起了医学健康研究中最重要的新兴领域之一:纳米医生(欧洲委员会,2020年)。Nanomedicine涉及使用纳米材料和纳米技术来解决疾病诊断,监测,控制,预防和治疗的挑战(Agrahari和Hiremath,2017,Patra等,2018,Soares等,2018,Tinkle等人,2014)。制备作为药物递送系统的纳米胺通常涉及活性药物成分,其封装在纳米尺寸载体基质(Murthy,2007)内包封或缀合。The carrier material can be based on inorganic (e.g., metal nanoparticles, semi-conductor quantum dots of various sizes and shapes (Biju et al., 2008, Tagit et al., 2015, Tagit et al., 2017, Tagit et al., 2011)) or organic nanostructures, including (and not limited to) polymers (Kumari et al., 2010), dendrimers (Gillies and Frechet, 2005), micelles (Kataoka et al., 2012), liposomes (Alavi et al., 2017), solid lipid nanoparticles (Mukherjee et al., 2009) and polymer-active pharmaceutical ingredient (API) conjugates (Larson and Ghandehari, 2012). These nanomedicines are finely engineered at the nanoscale to introduce various benefits such as protection of therapeutic agents from degradation, increased solubility and bioavailability, improved pharmacokinetics, reduced toxicity, enhanced therapeutic efficacy, decreased API immunogenicity, targeted delivery, and simultaneous diagnostics and treatment options with a single system (Agrahari and Hiremath, 2017, Patra et al., 2018).
为了达到所需的治疗效果,纳米载波应该:我)在血液室中运输过程中,要牢牢握住原料药,但是(二)一旦达到所需的目标,能够有效地释放API以发挥其药物作用。此外,运输车应该III)在血液隔室中是“隐蔽”,以有效地逃避网状内皮系统(RES)筛选,但iv)接触并穿透目标作用部位的正确细胞(Sun et al., 2012)。在这方面,基于聚(乳酸-共羟基乙酸)(PLGA)的纳米载体在设计和性能方面提供了巨大的机会,因为PLGA的各种特性使其成为理想的纳米载体(Han等人,2016,Makadia和Siegel, 2011, Singh等人,2014)。PLGA是一种可生物降解和生物相容的聚合物,降解时间可根据其分子量和共聚物比例进行调节。PLGA可溶于丙酮、氯化溶剂和乙酸乙酯等常见溶剂,可以加工成几乎任何形状和大小,并可以封装几乎任何大小的分子(Gentile et al., 2014, Makadia和Siegel, 2011, Södergård和Stolt, 2002)。因此,PLGA聚合物已被大量测试为药物、蛋白质和各种其他大分子(如DNA、RNA和肽)的运载工具(Jain, 2000, Makadia和Siegel, 2011)。除了聚合物的化学组成和分子量外,PLGA纳米载体的物理性质,如大小、形状、比体积比等,可以“调整”以获得所需的释放轮廓(Gentile et al., 2014, Makadia和Siegel, 2011)。
PLGA具有良好的生物相容性、可调的降解和释放特性以及高通用性,已被批准用于多种生物医学应用。事实上,尽管不是纳米,但目前市场上有超过60种基于plga的药物产品,具有不同的性质(即大小、形状等)。一些最知名的PLGA配方是基于微粒制剂的,如癸哌泰(市场上第一个基于雷公藤甲素的药品),Lupron depot®(醋酸亮丙雷啶),Nutropin depot®(生长激素),Suprecur®MP(醋酸布司林),Sandostatin®LAR depot(醋酸奥曲肽),Somatuline®LA(醋酸lanreotide), Trelstar™Depot (pamoate曲托瑞林),Vivitrol®(naltrexone)和Risperdal®Consta™(利培酮)。此外,基于plga的植入物(例如,分别基于醋酸戈瑟林、地塞米松、布塞林和比马前列素的Zoladex®、Ozurdex®、Profact®Depot、Durysta™等),甚至基于Atrigel®系统的原位成形植入物,即Eligard®(醋酸leuprolide) (Schwendeman et al., 2014)。基于plga的产品在市场上的大量存在表明了基于plga的纳米药物配方也有很好的前景。
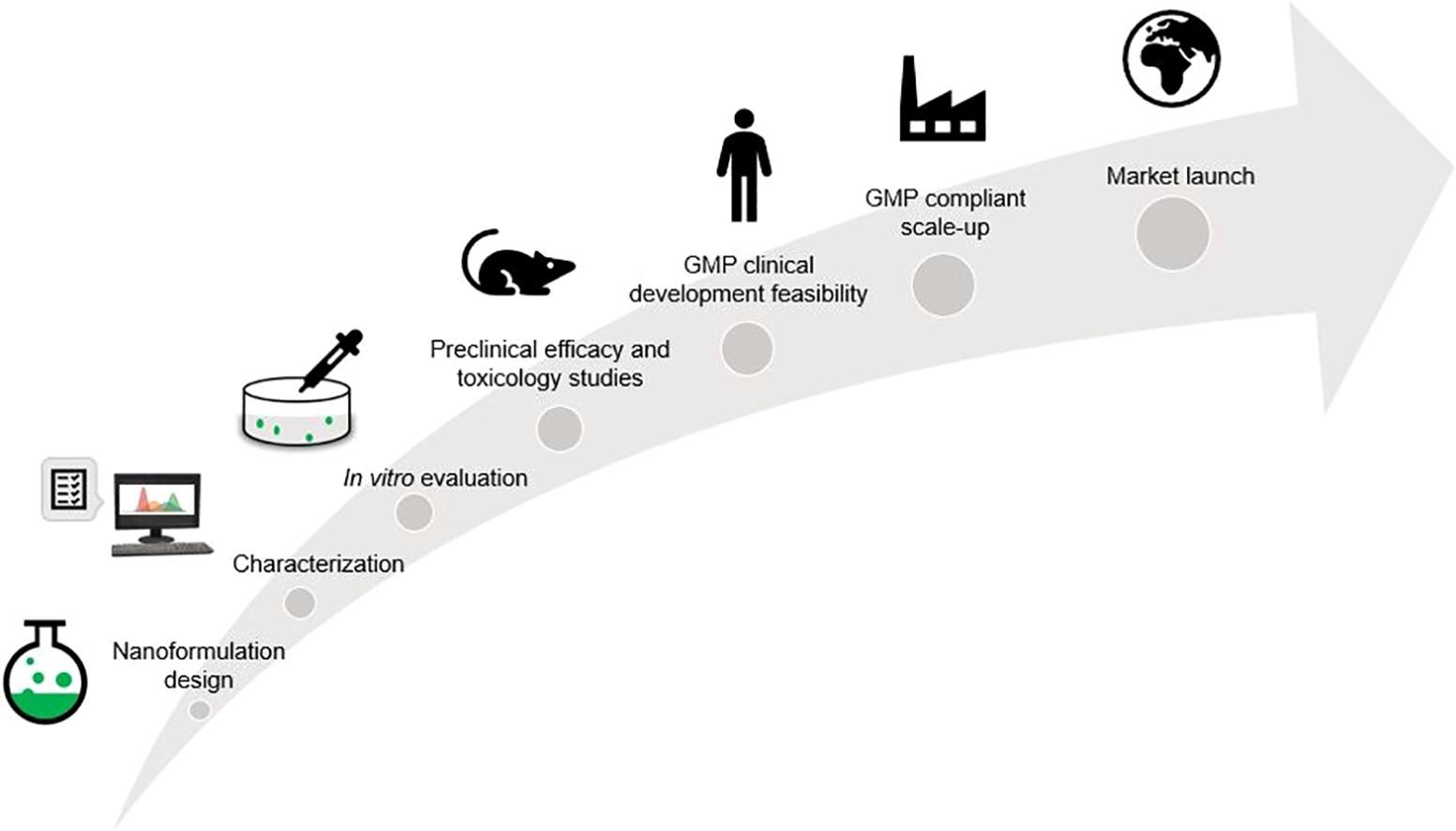
作为任何新的药物产品,PLGA的纳米胺类配方的发射包括从设计,实验室规模开发到扩大制造的复杂途径(图1)。The therapeutic efficacy and safety profile of nanomedicines need to be characterized through extensive (pre)clinical pharmacodynamics (i.e. efficacy and toxicity) and pharmacokinetics (i.e. biodistribution) studies in order to support the design and optimization of the nanomedicines (Havel et al., 2016).
除了治疗功效和安全性外,生产可扩展性是PLGA Nanomedicines的临床和商业开发的另一个关键要求,它与应用的制造技术密切相关(Agrahari和Agrahari,2018,Agrahari和Hiremath,2017,Paliwal等,2014)。然而,在从台式移动到大规模生产时出现挑战,因为与传统的药物产品不同,每个单独的纳米胺制剂的功效和安全性以及纳米颗粒的物理化学性质的直接后果携带API(MetSelaar和Lammers,2020),可以在采用更大的规模生产过程时改变。因此,除了建立良好制造实践的大规模过程之外 - (GMP)兼容的生产(Sun等,2012),需要使用各种表征技术的纳米载波的足够质量控制(QC)来确定是否直接放大或间接影响纳米型ines的临床表现(华等,2018)。
本研究概述了PLGA纳米颗粒的生产和分析的技术概述,妨碍了其工业实用性的扩大挑战以及与其成功翻译成诊所的问题。
文章信息:Maria Camilla Operti,Alexander Bernhardt,Silko Grimm,Andrea Engel,Carl Gustav Ficedor,Oya标记。基于plga的纳米药物制造:技术概述和工业放大的挑战,国际药物学报,第605卷,2021。https://doi.org/10.1016/j.ijpharm.2021.120807。

