聚l -赖氨酸多功能化黏膜穿透自乳化给药系统(SEDDS)的开发,提高环丙沙星对细胞内伤寒沙门氏菌的增溶和靶向给药
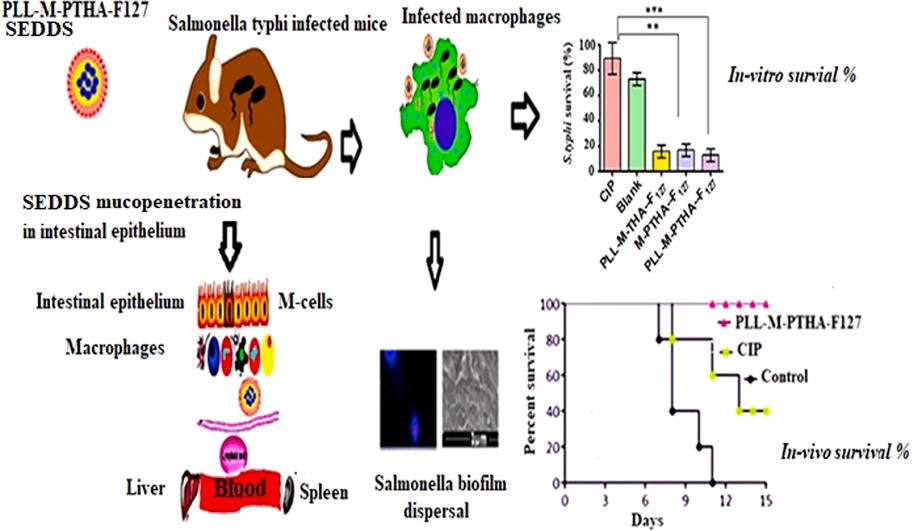
沙门氏菌伤寒由于当前抗生素环丙沙星(CIP)的溶解性和口服生物利用度较差,无法穿透巨噬细胞的胞内腔室,感染难以治疗。CIP的穿透和溶解能力差,导致胞内病原菌产生多药耐药,形成耐药生物膜。本研究开发了一种新型CIP靶向胞内的黏透自乳化给药系统(SEDDS)伤寒沙门氏菌具有高特异性和选择性的细菌。油的油,吐温80., 和挂钩基于增溶化容量和伪三元图乳化能力选择200作为油,表面活性剂和共表面活性剂。
突出了
粘液穿透两亲缀合物首次掺入潜水中。
多功能化的SEDDS对巨噬细胞显示无毒行为RAW 264.7。
SEDDS参与细胞内靶向杀伤伤寒杆菌。
比克服伤寒杆菌通过绕过非特异性药物传递的耐药性。
SEDDS被证明是一种很有前途的提高CIP增溶的载体。
通过加入聚l -赖氨酸功能化碳水化合物(甘露糖,预活化透明质酸)co-block pluronic F127 (PLL-M-PTHA-F127)聚合赋形剂,增强了SEDDS的黏透性。PLL-M-PTHA-F127是一种两亲性的粘膜穿透靶向抗菌生物实体,用于细胞内靶向伤寒沙门氏菌感染水库。采用动态光散射(DLS)、透射电子显微镜(TEM)、傅里叶变换红外光谱(FTIR)、差示扫描量热法(DSC)、紫外分光光度法(FTIR)、紫外分光光度法(DLS)、紫外分光光度法(DSC)、紫外分光光度法(FTIR)、紫外分光光度法(DSC)、紫外分光光度法(FTIR)对自纳米乳化载体进行表征。结果表明,pll - m - ptha - f127自纳米乳化给药系统(SEDDS)的水动力直径为247nm, PDI较低,zeta电势为负电荷。
在体外在下沉条件下,72h内药物缓释动力学为85%。CIP的PLL-M-PTHA-F127 SEDDS表现出很强的杀虫能力伤寒沙门氏菌与CIP相比,甚至以最低浓度的菌株,发现是血液相容性和生物相容性的。细胞内伤寒沙门氏菌与单独使用CIP相比,PLL-M-PTHA-F127 SEDDS的存活率最低。与其他配方和CIP相比,荧光显微镜图像证实了巨噬细胞胞腔内的熟练细胞摄取和快速胆石生物膜分散/清除活性。总之,PLL-M-PTHA-F127-SEDDS的CIP似乎是一个理想的候选根除伤寒沙门氏菌细胞内。
文章信息:Rabia Arshad,Tanveer A. Tabish,Abbas Ali Naseem,Muhammad Rauf Ul Hassan,Irshad Hussain,Shahzad Shaikh Hussain,Gul Shahnaz。分子液期杂志,2021. https://doi.org/10.1016/j.molliq.2021.115972。

